长肽合成技术
长肽合成通常指超过50个氨基酸的多肽的合成。长肽通常会采用基因表达及SDS-PAGE法来获得,但是这种方法周期长,最终产物分离效果差等,使固相法长肽合成技术成为一种需要。但是长肽的合成采用常规固相合成法的时候,随着肽链增长,偶联效率下降,副反应增多。长肽合成中,我们一直面临一个矛盾,即合成中随着序列的增长,缩合反应空间位阻增大,为了反应完全,需要增加反应时间;但是随着反应时间的延长,其产生的副反应就越多,一些缺残基的目标肽就随之产生。这些缺残基的肽链也是长肽合成过程中所产生的主要杂质。这些通常会导致多肽合成变得困难甚至导致长肽合成的失败。因此,长肽的合成过程中,我们需要克服的主要困难是探索更优质的反应条件和反应方法,从而使氨基酸缩合反应进行的更充分更彻底,同时缩短反应时间。肽研生物经过长期的摸索与积累,对合成工艺及方法不断优化,解决了长肽合成难,纯化难的问题,肽研生物长肽合成成功率高,质量稳定。
 提高长肽合成成功率的常用方法
提高长肽合成成功率的常用方法
1. 优化固相肽合成(SPPS)条件
-
树脂选择:根据多肽序列选择合适的树脂(如Wang树脂、Rink酰胺树脂),选用低取代度(Loading)的树脂;
-
偶联试剂:使用高效的偶联试剂(如HBTU/HATU/HOBt/DIPEA)提高偶联效率;
-
脱保护步骤:优化脱保护条件(如使用20% Piperidine/DMF)确保完全脱保护;
-
洗涤步骤:彻底洗涤树脂,去除未反应试剂和副产物;
2. 使用新型原料
-
使用异二肽或者伪二肽:伪二肽或者异二肽中类似脯氨酸(Pro)的五元环结构,可以打断多肽形成α-螺旋或者形成α-螺旋或的趋势,从而增加多肽的溶解性,特别是异二肽的使用,可以将溶解性增加的过程延长到多肽纯化结束,而临时形成的五元环结构可以通过调节pH让其还原为正常结构,从而在保证结构正确的前提下,让多肽更容易被纯化;
3. 分段合成与片段缩合
-
分段合成与片段缩合:当长肽合成用常规合成方法合成困难,可以将长肽分成较短的片段分别合成,减少单次合成的长度,然后通过HPLC纯化各片段,确保片段纯度,再使用高效的缩合剂(如HBTU/HOBt/DIPEA)进行片段缩合,优化反应条件(如溶剂、温度、pH);
-
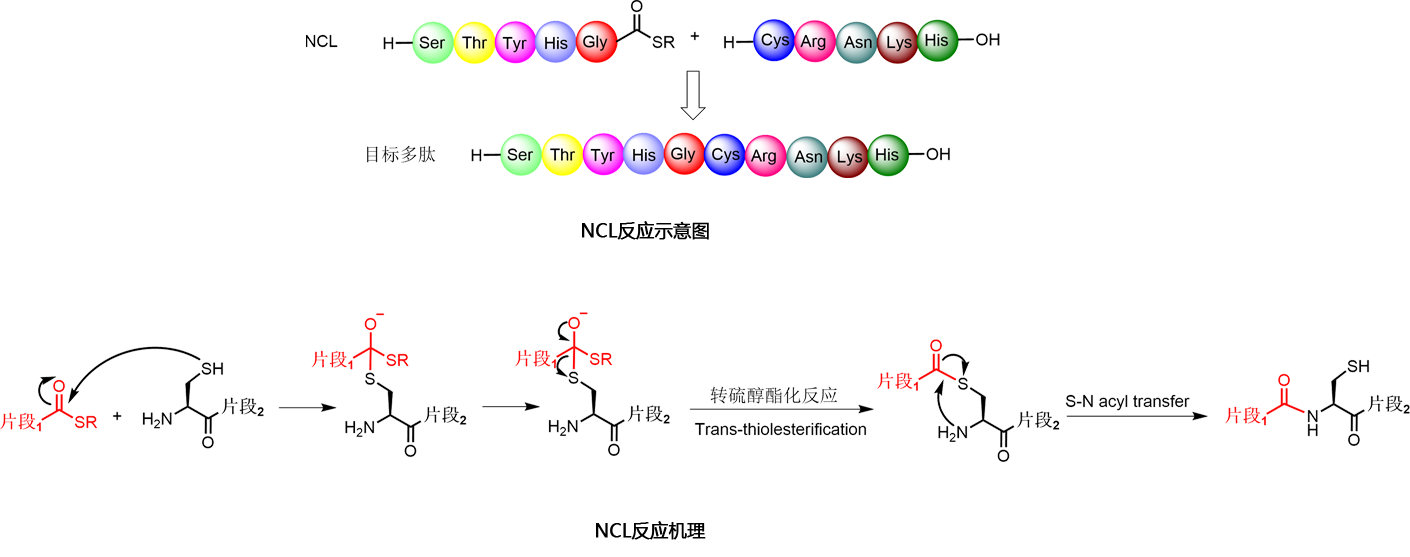
天然化学连接(NCL)片段法:天然化学连接(natural chemical ligation,NCL)是将两个未经保护的肽片段通过酰胺键组合成长肽或者蛋白质的反应,由德国的Theodor Wieland于1953年首次提出。NCL是蛋白质化学合成中使用最广泛的方法之一,广泛适用于200个氨基酸以下的蛋白质合成。与固相合成相比,NCL具有不需要缩合试剂和繁琐的保护基 (图1)、在水性缓冲液中即可反应等优势,还可以突破固相合成对于肽序列中氨基酸数目的限制,因此成为蛋白质合成领域的研究热点。该反应的机理是C端的硫酯与N端的巯基发生酯交换后生成新的硫酯中间体,然后经由五元环过渡态进行分子内S-N酰基迁移得到由半胱氨酸残基连接的多肽片段;
NCL法主要步骤分为三步:
1)C 端先形成硫酯,硫酯一般分为两种,烷基酯和苯基酯;
2)硫酯交换反应,C 端的硫酯和 N 端 Cys 的巯基进行交换,生成硫酯中间体,形成五元环;
3)S 到 N 的迁移,五元环迅速发生分子内酰基化转移,形成新的酰胺键即天然肽键。在此反应过程中无法检测到反应的中间体,因为酰基化转移的速度非常的快。
天然化学连接的优点有以下几点:
1)反应物多肽无需任何保护基团;
2)反应在中性的水溶液中,温度室温即可,条件相对温和;
3)由于此反应可以在浓度很低的情况下高效进行反应,因而解决了一些长肽的溶解性问题。
4. 监控和优化反应过程
-
实时监控:使用茚三酮,质谱(MS)或高效液相色谱(HPLC)实时监控反应过程,及时调整反应条件;
-
反应优化:根据监控结果,优化反应条件(如反应时间、温度、试剂浓度);
5. 采用微波合成法
-
采用微波合成法:对于合成过程中出现的一些难以缩合的氨基酸,我们采用微波法进行合成,该方法效果显著,并且大大缩短了反应时间,同时减少了两种主要副产物的产生;







 扫描添加微信联系我们
扫描添加微信联系我们 支持喀斯玛平台下单
支持喀斯玛平台下单 支持瑞竞平台下单
支持瑞竞平台下单







